Gli operatori sanitari si confrontano ogni giorno con la necessità di contenere i costi e migliorare l’efficienza, pur mantenendo standard elevati di cura e prevenendo la contaminazione incrociata. La sicurezza di pazienti e personale dipende dall’applicazione rigorosa delle procedure asettiche in sala operatoria. Tuttavia, nonostante queste misure, le infezioni continuano a rappresentare una sfida costante, anche negli ambienti più controllati.
Le infezioni associate all’assistenza sanitaria (HAI) rappresentano una criticità rilevante, sia in termini clinici sia economici, con le infezioni del sito chirurgico (SSI) tra le principali cause. L’incidenza delle SSI è influenzata da molteplici fattori, tra cui le condizioni del paziente, gli aspetti ambientali e le procedure operative. Microrganismi come batteri, virus e funghi possono contaminare l’ambiente chirurgico attraverso diverse vie, tra cui il personale sanitario, gli indumenti, le attrezzature o gli strumenti chirurgici. Anche il comportamento del team in sala operatoria è determinante: interruzioni della tecnica sterile, come una scarsa igiene delle mani, il mancato rispetto del campo sterile o la rottura dei guanti, aumentano significativamente il rischio di trasmissione di agenti patogeni al sito chirurgico.
Nonostante l’adozione di protocolli rigorosi, le infezioni restano una delle principali criticità in ambito chirurgico. Le infezioni del sito chirurgico (SSI) possono comportare un aumento del carico assistenziale, con ricoveri ospedalieri prolungati, maggior impiego di personale, utilizzo aggiuntivo di farmaci e dispositivi, maggiore consumo energetico e, in alcuni casi, la necessità di ulteriori interventi. Queste conseguenze si traducono in un incremento significativo dei costi sanitari, della morbilità e della mortalità, compromettendo la sostenibilità complessiva del sistema sanitario.
Incidenza dell'infezione
Si stima che un paziente su 20 sottoposto a intervento chirurgico sviluppi un’infezione del sito chirurgico (SSI)¹, mentre il tasso di esposizione del personale sanitario al sangue del paziente durante l’intervento è pari a 10,4 ogni 100 procedure². Garantire la sicurezza del paziente in sala operatoria, così come proteggere gli operatori sanitari dal rischio di infezioni da patogeni a trasmissione ematica, è una priorità fondamentale per ogni struttura sanitaria.
In Europa, le infezioni del sito chirurgico colpiscono mezzo milione di persone ogni anno e rappresentano un costo aggiuntivo pari a 19 miliardi di euro³.
Esposizione all'infezione
Gli operatori sanitari sono quotidianamente esposti al rischio di contatto con agenti patogeni, in particolare attraverso le ferite da ago, che si stima siano circa un milione ogni anno in Europa⁴. Queste esposizioni rappresentano una minaccia concreta di trasmissione di infezioni ematiche, come epatite B, epatite C e HIV, a seguito del contatto diretto con il sangue dei pazienti.
Il peso delle infezioni del sito chirurgico
Le infezioni del sito chirurgico (SSI) non solo comportano costi elevati per il sistema sanitario, ma causano anche dolore e traumi significativi per i pazienti. Un’infezione profonda, ad esempio, può richiedere un ricovero ospedaliero prolungato, con un conseguente aumento del tempo dedicato dal personale sanitario, dell’uso di farmaci, dispositivi e risorse energetiche e, in alcuni casi, la necessità di ulteriori interventi chirurgici. Oltre al costo umano ed economico, tutto ciò comporta anche un impatto ambientale rilevante. Molti di questi esiti, tuttavia, sarebbero prevenibili attraverso misure efficaci di controllo delle infezioni.
Le SSI sono causate dall’ingresso di batteri attraverso le incisioni praticate durante l’intervento chirurgico. I microrganismi patogeni possono penetrare nell’area chirurgica attraverso diverse vie:
- Dalla flora cutanea del paziente stesso
- Dal personale dela sala operatoria, inclusi chirurghi e assistenti
- Dall'ambiente circostante, ad esempio attraverso la caduta di particelle dall'alto
- Da superfici o strumenti contaminati utilizzati durante l'intervento5
Prevenire le SSI rappresenta una sfida complessa. Si stima, ad esempio, che circa un terzo della popolazione sia portatore naturale di Staphylococcus aureus, un batterio comunemente presente sulla pelle e nelle cavità nasali⁶. Alcuni ceppi di questo batterio, resistenti alla meticillina (MRSA), sono classificati come organismi multiresistenti e rappresentano una minaccia significativa in ambito ospedaliero. Sia gli stafilococchi che gli enterococchi sono in grado di sopravvivere per giorni o persino mesi una volta essiccati, anche su superfici comuni come tessuti e materiali plastici presenti negli ambienti ospedalieri. Questa persistenza ambientale ne aumenta il potenziale di trasmissione, rendendo ancora più cruciale l’adozione di rigorose misure di prevenzione e disinfezione⁷.
Anche l’aria rappresenta una fonte potenziale di contaminazione in sala operatoria. Gli esseri umani rilasciano migliaia di particelle cutanee ogni minuto⁸, ciascuna delle quali può veicolare microrganismi. Si stima che circa l’80% dei batteri presenti in un ambiente chirurgico provenga proprio dall’aria⁹, rendendo essenziale il controllo della qualità dell’aria mediante adeguati sistemi di ventilazione, filtrazione e contenimento.
Guanto per prevenire l'infezione
a prevenzione delle infezioni e della contaminazione incrociata in sala operatoria richiede un approccio globale, che consideri l’aria, i pazienti, il personale, le attrezzature e le superfici. Collaboriamo fianco a fianco con gli operatori sanitari per individuare e implementare le soluzioni più efficaci, con l’obiettivo comune di garantire la massima sicurezza in ogni fase del percorso chirurgico.
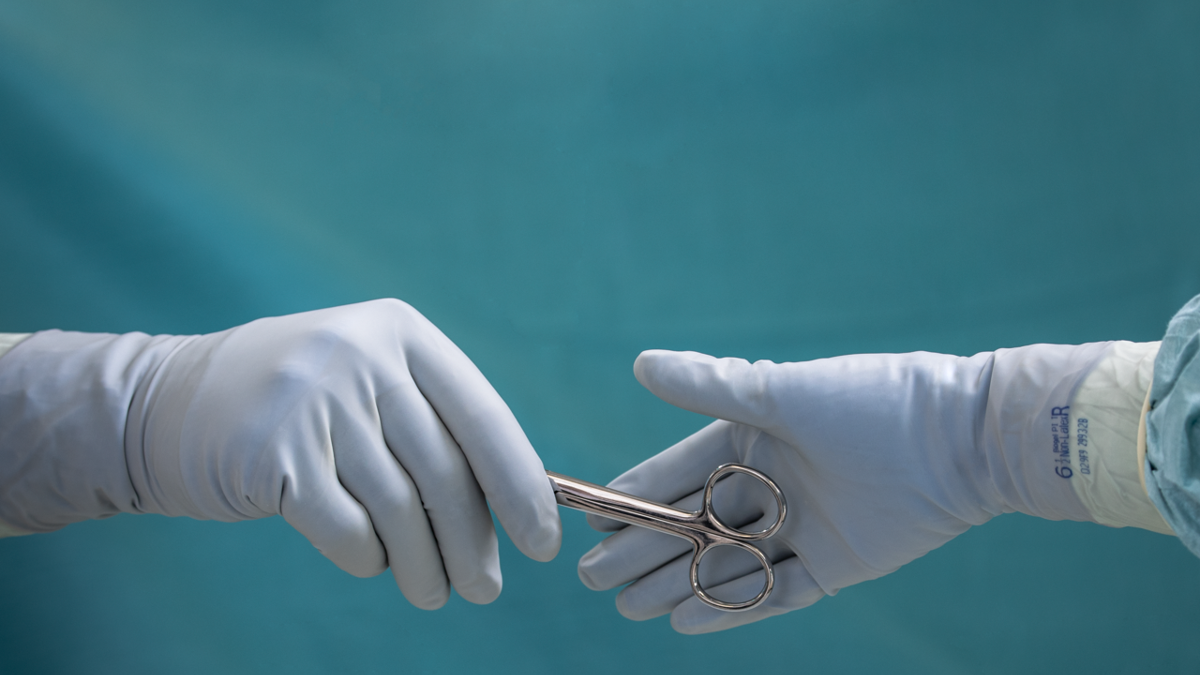
Guanti chirurgici
Guanto singolo:
I guanti chirurgici contribuiscono a ridurre il rischio di infezione sia per gli operatori sanitari che per i pazienti¹⁰,¹¹ e rappresentano uno dei numerosi elementi che cooperano per prevenire la contaminazione in sala operatoria¹⁰. Tuttavia, se un guanto viene perforato da un ago, la protezione viene compromessa e il danno può non essere visibile. La perforazione dei guanti è associata a un aumento del rischio di infezioni del sito chirurgico (SSI)¹¹.
La polvere utilizzata per facilitare l’inserimento e la rimozione dei guanti chirurgici può comportare rischi significativi, tra cui ridotta resistenza alle infezioni, contaminazione batterica ambientale, reazioni da corpo estraneo, ritardo nella guarigione delle ferite, formazione di aderenze e granulomi¹²,¹³. Tutte queste potenziali conseguenze possono aumentare il rischio di SSI¹⁴.
Doppio guanto con sistema di indicazione della foratura:
L’uso del doppio guanto con sistema di indicazione delle forature, composto da un sottoguanto e un sopraguanto, consente all’operatore sanitario di individuare immediatamente una perforazione. Questo permette una sostituzione rapida dei guanti, garantendo la continuità della procedura senza compromettere la protezione contro le infezioni crociate¹⁵,¹⁶.
In uno studio sui guanti utilizzati durante procedure chirurgiche, il tasso di rilevamento delle perforazioni è risultato pari al 90,2% con l’uso di guanti con sistema di indicazione, rispetto al 36,0% con doppio guanto standard (due guanti normali) e al 23,0% con guanti singoli¹⁵.
È stato dimostrato che l’impiego del doppio guanto riduce significativamente il rischio di punture da ago, ferite da taglio ed esposizione a infezioni trasmesse per via ematica. Una revisione Cochrane del 2014 ha evidenziato che il doppio guanto diminuisce del 71% la probabilità di perforazione del guanto interno rispetto all’uso di un solo guanto¹⁶.
Le principali autorità raccomandano oggi l’utilizzo del doppio guanto per gli interventi chirurgici invasivi:
- Centers for Disease Control and Prevention (CDC)¹⁷
- National Association of Theatre Nurses (NATN)¹⁸
- Association of periOperative Registered Nurses (AORN)¹⁹
- American College of Surgeons (ACS)²⁰
- Royal College of Surgeons of England¹⁸
- Australian College of Operating Room Nurses¹⁸
Prevenire l'infezione con l'abbigliamento per il personale
L'abbigliamento per il personale riveste un ruolo fondamentale nella prevenzione delle infezioni, contribuendo a proteggere sia i pazienti sia gli operatori dalla contaminazione e a mantenere la purezza dell'aria all'interno della sala operatoria.
Divise pluriuso (riutilizzabili)
Le divise tradizionali in tessuto vengono lavate e riutilizzate tra un intervento chirurgico e l’altro. Tuttavia, l’impiego di tessuti multipaziente (riutilizzabili) solleva dubbi sull’efficacia dei processi di sanificazione, sui rischi legati alla produzione di lanugine, sulle implicazioni per la salute e la sicurezza del personale, nonché sull’impatto ambientale.
Lavaggio delle divise pluriuso
Macchie, usura e pericoli invisibili come i batteri possono compromettere la protezione e la qualità delle prestazioni.
In primo luogo, è possibile garantire l’efficienza di una lavanderia, sia interna alla struttura sia affidata a terzi? Le evidenze mostrano che le lavanderie possono ospitare agenti patogeni anche in ambienti puliti, causando ricontaminazione dopo la disinfezione. In uno studio, un epidemiologo ha identificato il bucato come un potenziale vettore non riconosciuto di infezioni ospedaliere21.
La difficoltà di rimuovere efficacemente batteri recalcitranti, come il Clostridium difficile, è stata dimostrata in un grande ospedale universitario negli Stati Uniti. Sono stati rilevati alti livelli di CDIFF sia nelle aree sporche sia in quelle pulite della lavanderia, oltre che sulle maniglie dei camion che trasportavano i tessuti lavorati alla struttura22.
L’aumento del rischio di particelle sospese nell’aria legato al lavaggio è dovuto alla produzione di lanugine. Queste particelle aumentano il rischio di SSI e la contaminazione da lanugine delle ferite chirurgiche contribuisce a complicanze come trombogenesi (coaguli di sangue), infezioni, infiammazione amplificata, ritardo nella guarigione delle ferite, granulomi, aderenze e formazione di capsule.
Salute e sicurezza delle divise pluriuso
La salute sul lavoro è una componente fondamentale della sostenibilità e, di conseguenza, ridurre il rischio di esposizione a materiale contaminato è essenziale per garantire la sicurezza di tutto il personale. Nel caso dei prodotti tessili multipaziente (riutilizzabili), il lavaggio comporta rischi per la salute e la sicurezza sia per chi li indossa, sia per i pazienti e per il personale addetto alla lavanderia. Gli operatori delle lavanderie ospedaliere, ad esempio, maneggiano ripetutamente questi prodotti e sono esposti al rischio di contatto con materiale contaminato e di infezioni.
Impatto ambientale delle divise (riutilizzabili)
Le tute chirurgiche multipaziente (riutilizzabili) presentano anche un impatto ambientale significativo. L’impronta ecologica associata al loro riciclo include il consumo di acqua, l’immissione nelle acque reflue di agenti patogeni AMR, biocidi e detergenti. Le lavanderie, inoltre, richiedono grandi quantità di acqua calda, con un elevato dispendio energetico: si stima che utilizzino circa il 50-75% dell’acqua calda complessivamente generata da un ospedale. Anche le attività di trasporto e consegna della biancheria contribuiscono ulteriormente alle emissioni di CO₂.
Divise monouso
Le divise monouso contribuiscono alle misure di controllo delle infezioni ospedaliere. Le divise in polipropilene, in particolare, sono associate a una contaminazione batterica dell’aria e delle ferite significativamente inferiore rispetto a camicie e pantaloni in cotone convenzionali.
Indossare divise monopaziente garantisce che chi le utilizza abbia sempre un prodotto nuovo e di qualità controllata, senza rischi di danni o contaminazioni derivanti da un uso precedente.
Clean air suits
L’aria pulita in sala operatoria si ottiene grazie a una combinazione di flusso d’aria laminare, numero di aperture delle porte, numero di persone presenti e utilizzo di specifiche divise. Questo è particolarmente importante negli interventi ortopedici, implantari e pediatrici.
Le clean air suits sono specificamente progettate per ridurre la contaminazione da microrganismi presenti nell’aria da parte del personale. Offrono una protezione superiore rispetto ai sistemi multipaziente (riutilizzabili) in cotone/poliestere, garantendo un’elevata resistenza alla penetrazione batterica, anche con ventilazione ordinaria in sala operatoria.
Prevenire la contaminazione dalla cute del paziente
I teli chirurgici e il lavaggio di tutto il corpo possono impedire ai microrganismi della cute del paziente di contaminare la ferita chirurgica e causare SSI.

Teli chirurgici
I teli chirurgici impediscono il trasferimento di microrganismi dalla cute del paziente durante le procedure chirurgiche. I materiali impermeabili contribuiscono al controllo delle infezioni, mentre un’efficace gestione dei fluidi mantiene l’area di lavoro più asciutta. I teli più efficienti sono progettati con un numero ridotto di componenti e sono facili da utilizzare, al fine di ridurre il rischio di contaminazione.
Lavare la cute
Il lavaggio dell’intero corpo riduce la carica batterica cutanea e, di conseguenza, diminuisce il rischio di infezioni del sito chirurgico (SSI). Esistono diversi metodi per detergere la cute:
-
Acqua e sapone: la procedura standard più comune per la pulizia del paziente, ma tende semplicemente a diffondere gli organismi, spostando i batteri dalle aree naturalmente più colonizzate sulla superficie della cute30.
-
Iodio povidone: il lavaggio preoperatorio con iodio povidone offre una certa protezione, ma la presenza di sostanze associate alla chirurgia come sangue, secrezioni e grasso ne riduce l’efficacia31.
-
Soluzione di clorexidina digluconato: vari studi hanno dimostrato che questa soluzione previene le infezioni acquisite in ambito sanitario, in particolare in terapia intensiva32. I protocolli chirurgici recenti raccomandano di effettuare due docce con clorexidina digluconato prima dell’intervento, lasciando agire la soluzione per almeno un minuto prima di risciacquare33. Inoltre, provoca meno reazioni cutanee rispetto ad altre alternative34.
Riduzione dei potenziali vettori di infezione con i set procedurali
Oltre ad aumentare l'efficienza e la praticità, i ProcedurePak riducono il potenziale di introduzione di ulteriori fonti di microrganismi nella sala operatoria35. Tutti i componenti, gli strumenti chirurgici, i teli e i camici specifici per la procedura necessari per eseguire un intervento chirurgico sono contenuti in un’unica confezione. Questa confezione rappresenta non solo una base per ridurre i tempi di preparazione, apertura e configurazione³⁸, ma anche per diminuire il rischio di contaminazione in sala operatoria, grazie al minor numero di confezioni da aprire³⁹.
Tutto in uno e monouso
ProcedurePak è progettato per includere ogni singolo componente necessario per una singola procedura chirurgica all’interno di un’unica confezione, il che significa meno confezioni da aprire, meno sprechi in sala operatoria36 e minori rischi di contaminazione37.
La comodità “all-in-one” di ProcedurePak consente inoltre una configurazione più rapida della sala operatoria, contribuendo a una riduzione complessiva della durata della procedura, fattore che ha dimostrato di ridurre il rischio di SSI.



